Aromatic HCs (สนามกีฬา)คือไฮโดรคาร์บอนที่โมเลกุลประกอบด้วยวงแหวนเบนซีนตั้งแต่หนึ่งวงขึ้นไป
ตัวอย่างของอะโรมาติกไฮโดรคาร์บอน:

สนามกีฬาแถวเบนซิน (สนามกีฬาโมโนไซคลิก)
สูตรทั่วไป: C n H 2n-6 , n≥6
ตัวแทนที่ง่ายที่สุดของอะโรมาติกไฮโดรคาร์บอนคือเบนซินสูตรเชิงประจักษ์คือ C 6 H 6 .
โครงสร้างอิเล็กทรอนิกส์ของโมเลกุลเบนซีน
สูตรทั่วไปของ C n H 2 n -6 โมโนไซคลิก arenes แสดงให้เห็นว่าพวกมันเป็นสารประกอบไม่อิ่มตัว
ในปี ค.ศ. 1856 นักเคมีชาวเยอรมัน A.F. Kekule เสนอสูตรไซคลิกสำหรับเบนซินที่มีพันธะคอนจูเกต (พันธะเดี่ยวและพันธะคู่สลับกัน) - cyclohexatriene-1,3,5: 
โครงสร้างของโมเลกุลเบนซีนนี้ไม่ได้อธิบายคุณสมบัติหลายอย่างของเบนซีน:
- สำหรับน้ำมันเบนซิน ปฏิกิริยาการแทนที่เป็นคุณลักษณะเฉพาะ และไม่ใช่ลักษณะเฉพาะของปฏิกิริยาการเติมของสารประกอบที่ไม่อิ่มตัว ปฏิกิริยาการเติมเป็นไปได้ แต่ยากกว่าสำหรับ
- เบนซินไม่ทำปฏิกิริยาที่ ปฏิกิริยาเชิงคุณภาพเป็นไฮโดรคาร์บอนไม่อิ่มตัว (ด้วยน้ำโบรมีนและสารละลาย KMnO 4)
ภายหลังการศึกษาการเลี้ยวเบนของอิเล็กตรอนพบว่าพันธะทั้งหมดระหว่างอะตอมของคาร์บอนในโมเลกุลเบนซีนมีความยาวเท่ากันคือ 0.140 นาโนเมตร (ค่าเฉลี่ยระหว่างความยาวของอะตอมธรรมดา การเชื่อมต่อ CC 0.154 นาโนเมตรและพันธะคู่ C=C 0.134 นาโนเมตร) มุมระหว่างพันธะที่อะตอมของคาร์บอนแต่ละอะตอมคือ 120° โมเลกุลเป็นรูปหกเหลี่ยมแบนปกติ
ทฤษฎีสมัยใหม่เพื่ออธิบายโครงสร้างของโมเลกุล C 6 H 6 ใช้แนวคิดเรื่องไฮบริไดเซชันของออร์บิทัลของอะตอม
อะตอมของคาร์บอนในน้ำมันเบนซินอยู่ในสถานะของการผสมแบบ sp 2 อะตอม "C" แต่ละตัวสร้างพันธะ σ สามพันธะ (สองอะตอมมีอะตอมของคาร์บอนและอีกอะตอมหนึ่งมีอะตอมไฮโดรเจน) พันธะ σ ทั้งหมดอยู่ในระนาบเดียวกัน:
อะตอมของคาร์บอนแต่ละอะตอมมีอิเล็กตรอน p หนึ่งตัว ซึ่งไม่มีส่วนร่วมในการผสมพันธุ์ p-orbitals ที่ไม่ผสมพันธุ์ของอะตอมคาร์บอนอยู่ในระนาบ ตั้งฉากกับระนาบσ-พันธบัตร p-cloud แต่ละอันทับซ้อนกันกับ p-clouds สองอันที่อยู่ใกล้เคียงและด้วยเหตุนี้ π-system คอนจูเกตเดียวจึงเกิดขึ้น (จำผลกระทบของการผันกันของ p-electron ในโมเลกุล 1,3-butadiene ที่กล่าวถึงในหัวข้อ “Diene ไฮโดรคาร์บอน”):
การรวมกันของพันธะ σ 6 ตัวกับระบบ π เดียว เรียกว่า พันธะอะโรมาติก
วงแหวนคาร์บอน 6 อะตอม เชื่อมกันด้วยพันธะอะโรมาติก เรียกว่า แหวนเบนซิน,หรือ นิวเคลียสของเบนซิน.
ตามแนวคิดสมัยใหม่เกี่ยวกับโครงสร้างอิเล็กทรอนิกส์ของเบนซิน โมเลกุล C 6 H 6 มีดังต่อไปนี้

คุณสมบัติทางกายภาพของน้ำมันเบนซิน
น้ำมันเบนซินภายใต้สภาวะปกติเป็นของเหลวไม่มีสี t o pl = 5.5 o C; ทีโอคิป = 80 เกี่ยวกับ C; มีกลิ่นเฉพาะตัว ผสมกับน้ำ ตัวทำละลายดี เป็นพิษสูง.
คุณสมบัติทางเคมีของเบนซิน
พันธะอะโรมาติกเป็นตัวกำหนดคุณสมบัติทางเคมีของเบนซีนและอะโรมาติกไฮโดรคาร์บอนอื่นๆ
ระบบอิเล็กตรอน 6π มีความเสถียรมากกว่าพันธะ π สองอิเล็กตรอนทั่วไป ดังนั้นปฏิกิริยาการเติมจึงเป็นเรื่องปกติสำหรับอะโรมาติกไฮโดรคาร์บอนมากกว่าไฮโดรคาร์บอนที่ไม่อิ่มตัว โดยทั่วไปมากที่สุดสำหรับ arenes คือปฏิกิริยาการทดแทน
ฉัน. ปฏิกิริยาการทดแทน
1.ฮาโลเจน

2. ไนเตรชั่น
ปฏิกิริยาจะดำเนินการด้วยของผสมของและกรด (ของผสมไนเตรต): 
3. ซัลโฟเนชั่น

4. Alkylation (แทนที่อะตอม "H" ด้วยหมู่อัลคิล) - ปฏิกิริยาของ Friedel-Craftsเกิดคล้ายคลึงกันของน้ำมันเบนซิน:

แทนที่จะใช้ฮาโลอัลเคน สามารถใช้อัลคีนได้ (ต่อหน้าตัวเร่งปฏิกิริยา - AlCl 3 หรือกรดอนินทรีย์):

II. ปฏิกิริยาการเติม
1. ไฮโดรจีเนชัน

2. การเติมคลอรีน

สาม.ปฏิกิริยาออกซิเดชัน
1. การเผาไหม้
2C 6 H 6 + 15O 2 → 12CO 2 + 6H 2 O
2. ไม่ การเกิดออกซิเดชันที่สมบูรณ์ (KMnO 4 หรือ K 2 Cr 2 O 7 ในสภาพแวดล้อมที่เป็นกรด) แหวนเบนซินมีความทนทานต่อสารออกซิไดซ์ ปฏิกิริยาจะไม่เกิดขึ้น
รับน้ำมันเบนซิน
ในอุตสาหกรรม:
1) การแปรรูปน้ำมันและถ่านหิน
2) ดีไฮโดรจีเนชันของไซโคลเฮกเซน:

3) dehydrocyclization (aromatization) ของเฮกเซน:

ในห้องปฏิบัติการ:
การรวมเกลือของกรดเบนโซอิกกับ:

Isomerism และศัพท์เฉพาะของน้ำมันเบนซินคล้ายคลึงกัน
คล้ายคลึงกันเบนซินใด ๆ มีโซ่ด้านข้างเช่น อนุมูลอัลคิลติดอยู่กับวงแหวนเบนซีน คล้ายคลึงกันของเบนซีนแรกคือนิวเคลียสของเบนซีนที่เชื่อมโยงกับเมทิลเรดิคัล: 
โทลูอีนไม่มีไอโซเมอร์ เนื่องจากตำแหน่งทั้งหมดในวงแหวนน้ำมันเบนซินมีค่าเท่ากัน
สำหรับความคล้ายคลึงกันของเบนซีนที่ตามมา อาจมีไอโซเมอร์ได้หนึ่งประเภท - ไอโซเมอร์ของสายโซ่ด้านข้าง ซึ่งสามารถเป็นได้สองประเภท:
1) isomerism ของจำนวนและโครงสร้างของหมู่แทนที่
2) isomerism ของตำแหน่งของสารทดแทน



คุณสมบัติทางกายภาพของโทลูอีน
โทลูอีน- ของเหลวไม่มีสีมีกลิ่นเฉพาะตัว ไม่ละลายในน้ำ ละลายได้ในตัวทำละลายอินทรีย์ โทลูอีนเป็นพิษน้อยกว่าเบนซีน
คุณสมบัติทางเคมีของโทลูอีน
ฉัน. ปฏิกิริยาการทดแทน
1. ปฏิกิริยาที่เกี่ยวกับวงแหวนเบนซิน
เมทิลเบนซีนเข้าสู่ปฏิกิริยาการแทนที่ทั้งหมดที่เกี่ยวข้องกับเบนซีน และในขณะเดียวกันก็แสดงปฏิกิริยาที่สูงกว่า ปฏิกิริยาดำเนินไปในอัตราที่เร็วขึ้น
เมทิลเรดิคัลที่มีอยู่ในโมเลกุลโทลูอีนเป็นสารทดแทนในสกุล ดังนั้น อันเป็นผลมาจากปฏิกิริยาการแทนที่ในนิวเคลียสของเบนซีน อนุพันธ์ของโทลูอีนออร์โธและพาราไดซ์จะได้รับหรือมีรีเอเจนต์มากเกินไป อนุพันธ์ไตร ของสูตรทั่วไป:

ก) ฮาโลเจน


ด้วยคลอรีนเพิ่มเติม สามารถรับไดคลอโรเมทิลเบนซีนและไตรคลอโรเมทิลเบนซีนได้:

II. ปฏิกิริยาการเติม
ไฮโดรจิเนชัน

สาม.ปฏิกิริยาออกซิเดชัน
1. การเผาไหม้
C 6 H 5 CH 3 + 9O 2 → 7CO 2 + 4H 2 O
2. การเกิดออกซิเดชันที่ไม่สมบูรณ์
ไม่เหมือนน้ำมันเบนซิน homologues ของมันถูกออกซิไดซ์โดยตัวออกซิไดซ์บางชนิด ในกรณีนี้ โซ่ข้างจะเกิดปฏิกิริยาออกซิเดชัน ในกรณีของโทลูอีน คือ กลุ่มเมทิล ตัวออกซิไดซ์อย่างอ่อน เช่น MnO 2 ออกซิไดซ์ไปเป็นหมู่อัลดีไฮด์ ตัวออกซิไดซ์ที่แรงกว่า (KMnO 4) ทำให้เกิดออกซิเดชันต่อกรด: 
คล้ายคลึงกันของเบนซินที่มีสายโซ่ด้านเดียวถูกออกซิไดซ์โดยตัวออกซิไดซ์ที่แรง เช่น KMnO4 กับกรดเบนโซอิก กล่าวคือ มีการแตกในโซ่ด้านข้างด้วยการเกิดออกซิเดชันของส่วนที่แยกออกเป็น CO 2; ตัวอย่างเช่น: 
เมื่อมีโซ่ด้านข้างหลายสาย โซ่แต่ละอันจะถูกออกซิไดซ์เป็นหมู่คาร์บอกซิล และเป็นผลให้กรดโพลีเบสิกก่อตัวขึ้น ตัวอย่างเช่น

รับโทลูอีน:
ในอุตสาหกรรม:
1) การแปรรูปน้ำมันและถ่านหิน
2) ดีไฮโดรจีเนชันของเมทิลไซโคลเฮกเซน:

3) dehydrocyclization ของเฮปเทน:
ในห้องปฏิบัติการ:
1) อัลคิเลชั่นของ Friedel-Crafts;
2) ปฏิกิริยาของเวิร์ตซ์-ฟิตทิก(ปฏิกิริยาของโซเดียมที่มีส่วนผสมของฮาโลเบนซีนและฮาโลอัลเคน).
เรานำเสนอวิดีโอสอนเกี่ยวกับหัวข้อ " คุณสมบัติทางเคมีน้ำมันเบนซิน" เมื่อใช้วิดีโอนี้ คุณจะเข้าใจถึงคุณสมบัติทางเคมีของน้ำมันเบนซิน ตลอดจนสภาวะที่ไม่เอื้ออำนวยซึ่งน้ำมันเบนซินต้องทำปฏิกิริยากับสารอื่นๆ
เรื่อง:อะโรมาติกไฮโดรคาร์บอน
บทเรียนหรือสอนหรือการเรียนและเครื่องเตือนสติ:คุณสมบัติทางเคมีของเบนซิน
ข้าว. 1. โมเลกุลเบนซีน
การทำลายเมฆ p-electron ในโมเลกุลของเบนซินนั้นทำได้ยาก ดังนั้นน้ำมันเบนซินจึงเข้าสู่ปฏิกิริยาเคมีน้อยกว่าสารประกอบไม่อิ่มตัวอย่างมาก


เพื่อให้น้ำมันเบนซินทำปฏิกิริยาเคมี จำเป็นต้องมีสภาวะที่ค่อนข้างรุนแรง: อุณหภูมิที่สูงขึ้น และในหลายกรณีก็ต้องใช้ตัวเร่งปฏิกิริยา ในปฏิกิริยาส่วนใหญ่ แหวนเบนซินที่เสถียรจะยังคงอยู่
1. โบรมิเน

ต้องใช้ตัวเร่งปฏิกิริยา (เหล็ก (III) หรืออะลูมิเนียมโบรไมด์) และต้องไม่ปล่อยน้ำปริมาณเล็กน้อยแม้แต่น้อย บทบาทของตัวเร่งปฏิกิริยาคือโมเลกุลโบรมีนถูกดึงดูดโดยอะตอมของโบรมีนหนึ่งอะตอมไปยังอะตอมของเหล็ก เป็นผลให้มันโพลาไรซ์ - อิเล็กตรอนพันธะคู่หนึ่งส่งผ่านไปยังอะตอมโบรมีนที่เกี่ยวข้องกับเหล็ก:
บรา+…. Br - ก.พ. 3 .
Br+ เป็นอิเล็กโทรฟิลที่แข็งแกร่ง วงแหวนเบนซีนดึงดูดเมฆหกอิเล็กตรอนและแตกตัว ทำให้เกิดพันธะโควาเลนต์กับอะตอมของคาร์บอน:
ไอออนโบรมีนสามารถเข้าร่วมกับไอออนบวกที่ได้ แต่การลดลงของระบบอะโรมาติกของวงแหวนเบนซีนนั้นดีกว่าการเติมแอนไอออนของโบรมีน ดังนั้นโมเลกุลจะเข้าสู่สภาวะเสถียรโดยการปล่อยไฮโดรเจนไอออนออกไป:
ปฏิกิริยาการแทนที่ด้วยไฟฟ้าทั้งหมดในวงแหวนเบนซินดำเนินการตามกลไกที่คล้ายกัน
2. ไนเตรชั่น

เบนซีนและสารที่คล้ายคลึงกันทำปฏิกิริยากับส่วนผสมของกรดซัลฟิวริกเข้มข้นและกรดไนตริก (ส่วนผสมไนเตรต) ในส่วนผสมไนเตรต ในสภาวะสมดุล มีไนโตรเนียมไอออน NO 2 + ซึ่งเป็นอิเล็กโทรไฟล์:

3. ซัลโฟเนชั่น
เบนซีนและ arenes อื่น ๆ เมื่อถูกความร้อนทำปฏิกิริยากับกรดซัลฟิวริกเข้มข้นหรือโอเลี่ยม - สารละลายของ SO 3 ในกรดซัลฟิวริก:

4 . Friedel-Crafts Alkylation
5. Alkylation กับ alkenes

ปฏิกิริยาเหล่านี้ไม่เอื้ออำนวยต่อความกระตือรือร้น ดังนั้นจะเกิดขึ้นเมื่อถูกความร้อนหรือฉายรังสีเท่านั้น
1. ไฮโดรจีเนชัน
เมื่อถูกความร้อน ที่ความดันสูงและต่อหน้าตัวเร่งปฏิกิริยา Ni, Pt หรือ Pd น้ำมันเบนซินและสารอื่น ๆ จะเติมไฮโดรเจนเพื่อสร้างไซโคลเฮกเซน:

2. คลอรีนจากน้ำมันเบนซิน
ภายใต้การกระทำของรังสีอัลตราไวโอเลต เบนซินจะเติมคลอรีน หากกระติกน้ำแก้วควอทซ์ที่มีสารละลายคลอรีนในเบนซีนสัมผัสกับแสงแดด สารละลายจะเปลี่ยนสีอย่างรวดเร็ว คลอรีนจะรวมตัวกับเบนซีนเพื่อสร้าง 1,2,3,4,5,6-เฮกซาคลอโรไซโคลเฮกเซน ซึ่งเรียกว่า เฮกซาคลอเรน(ก่อนหน้านี้ใช้เป็นยาฆ่าแมลง):

3. การเผาไหม้น้ำมันเบนซิน.
เปลวไฟของน้ำมันเบนซินและอะโรมาติกไฮโดรคาร์บอนอื่น ๆ นั้นแตกต่างจากอัลเคนและมีควัน
สรุปบทเรียน
ในบทเรียนนี้ คุณได้ศึกษาหัวข้อ "คุณสมบัติทางเคมีของน้ำมันเบนซิน" ด้วยการใช้วัสดุนี้ คุณสามารถเข้าใจถึงคุณสมบัติทางเคมีของเบนซิน รวมถึงสภาวะที่รุนแรงซึ่งน้ำมันเบนซินต้องทำปฏิกิริยากับสารอื่นๆ
บรรณานุกรม
1. Rudzitis G.E. เคมี. พื้นฐาน เคมีทั่วไป. ชั้นประถมศึกษาปีที่ 10: ตำราเรียนสำหรับ สถาบันการศึกษา: ระดับพื้นฐานของ/ G. E. Rudzitis, F.G. เฟลด์แมน - รุ่นที่ 14 - ม.: การศึกษา, 2555.
2. เคมี. เกรด 10 ระดับโปรไฟล์: การศึกษา เพื่อการศึกษาทั่วไป สถาบัน / V.V. Eremin, N.E. Kuzmenko, V.V. Lunin และคนอื่น ๆ - M .: Drofa, 2008. - 463 p.
3. เคมี. ชั้นประถมศึกษาปีที่ 11 ระดับโปรไฟล์: ตำราเรียน เพื่อการศึกษาทั่วไป สถาบัน / V.V. Eremin, N.E. Kuzmenko, V.V. Lunin และอื่น ๆ - M .: Drofa, 2010. - 462 p.
4. Khomchenko G.P. , Khomchenko I.G. ประมวลปัญหาเคมีสำหรับผู้ที่เข้ามหาวิทยาลัย - ครั้งที่ 4 - M .: RIA "New Wave": Publisher Umerenkov, 2012. - 278 p.
การบ้าน
1. หมายเลข 13, 14 (หน้า 62) Rudzitis G.E. , Feldman F.G. เคมี: เคมีอินทรีย์. เกรด 10: ตำราเรียนสำหรับสถาบันการศึกษา: ระดับพื้นฐาน / G. E. Rudzitis, F.G. เฟลด์แมน - รุ่นที่ 14 - ม.: การศึกษา, 2555.
2. ทำไมสารประกอบอะโรมาติกจึงมีสมบัติทางเคมีแตกต่างจากไฮโดรคาร์บอนทั้งแบบอิ่มตัวและไม่อิ่มตัว
3. เขียนสมการปฏิกิริยาการเผาไหม้ของเอทิลเบนซีนและไซลีน
   |
|
| เป็นระบบ ชื่อ | เบนซิน |
| ตัวย่อ | PhH |
| ชื่อดั้งเดิม | เครื่องเป่าผม (Laurent, 1837), ฟีนิลไฮโดรเจน เบนซิน |
| เคมี. สูตร | C₆H₆ |
| สถานะ | ของเหลว |
| มวลกราม | 78.11 ก./โมล |
| ความหนาแน่น | 0.8786 ก./ซม.³ |
| ความหนืดไดนามิก | 0.0652 ปะ ส |
| พลังงานไอออไนซ์ | 9.24 ± 0.01 eV |
| ต. ละลาย. | 5.5 ° |
| ต. กิ๊บ. | 80.1° |
| ต. รอบ | -11° |
| ต. svsp. | 562° |
| เป็นต้น ระเบิด | 1.2 ± 0.1 ปริมาตร% |
| แรงดันไอน้ำ | 75 ± 1 mmHg |
| การละลายในน้ำ | 0.073 ก./100 มล. |
| GOST | GOST 5955-75 |
| ทะเบียน หมายเลข CAS | 71-43-2 |
| PubChem | 241 |
| ทะเบียน หมายเลข EINECS | 200-753-7 |
| ยิ้ม | C1=CC=CC=C1 |
| InChI | |
| RTECS | CY1400000 |
| เชบิ | 16716 |
| เคมีแมงมุม | 236 |
| ความเป็นพิษ | เป็นพิษ มีคุณสมบัติเป็นสารก่อมะเร็งและเสพติด |
| คำสัญญาณ | อันตราย! |
| ข้อมูลจะได้รับสำหรับเงื่อนไขมาตรฐาน (25°, 100 kPa) เว้นแต่จะระบุไว้เป็นอย่างอื่น | |
คุณสมบัติทางเคมี
ปฏิกิริยาการทดแทนเป็นลักษณะของเบนซีน - เบนซินทำปฏิกิริยากับแอลคีน, คลอโรอัลเคน, ฮาโลเจน, กรดไนตริกและกรดซัลฟิวริก ปฏิกิริยาการแตกตัวของวงแหวนเบนซีนเกิดขึ้นภายใต้สภาวะที่ไม่เอื้ออำนวย (อุณหภูมิ ความดัน)
- ปฏิกิริยากับแอลคีน (อัลคิเลชั่น) อันเป็นผลมาจากปฏิกิริยาทำให้เกิดคล้ายคลึงกันของเบนซีนเช่นเอทิลเบนซีนและคิวมีน:
- ปฏิกิริยากับคลอรีนและโบรมีนต่อหน้าตัวเร่งปฏิกิริยาเพื่อสร้างคลอโรเบนซีน (ปฏิกิริยาการแทนที่ด้วยไฟฟ้า):
- ในกรณีที่ไม่มีตัวเร่งปฏิกิริยา เมื่อถูกความร้อนหรือส่องสว่าง ปฏิกิริยาการเติมที่รุนแรงจะเกิดขึ้นกับการก่อตัวของส่วนผสมของไอโซเมอร์เฮกซาคลอโรไซโคลเฮกเซน
- เมื่อเบนซีนทำปฏิกิริยากับโบรมีนในสารละลายโอเลี่ยม จะเกิดเฮกซาโบรโมเบนซีน:
- ปฏิกิริยากับอัลเคนที่เป็นฮาโลจิเนต (เบนซีน alkylation, ปฏิกิริยาของ Friedel-Crafts) เพื่อสร้างอัลคิลเบนซีน:

- ปฏิกิริยาอะซิเลชันของ Friedel-Crafts ของเบนซีนแอนไฮไดรด์, กรดคาร์บอกซิลิกเฮไลด์นำไปสู่การก่อตัวของอะโรมาติกคีโตนอะโรมาติกและไขมัน:

6 6 + 6 5 COCl → AlCl 3 6 5 COC 6 5 + HCl
ในปฏิกิริยาที่หนึ่งและสองจะเกิด acetophenone (เมทิลฟีนิลคีโตน) แทนอะลูมิเนียมคลอไรด์ด้วยพลวงคลอไรด์ทำให้อุณหภูมิของปฏิกิริยาลดลงเหลือ 25 องศาเซลเซียส ในปฏิกิริยาที่สามจะเกิดเบนโซฟีโนน (ไดฟีนิลคีโตน)
- ปฏิกิริยาการก่อตัว - อันตรกิริยาของเบนซีนที่มีส่วนผสมของ CO และ HCl เกิดขึ้นที่แรงดันสูงและภายใต้การกระทำของตัวเร่งปฏิกิริยา ผลิตภัณฑ์จากปฏิกิริยาคือเบนซาลดีไฮด์:
- ปฏิกิริยาซัลโฟเนชันและไนเตรต (การแทนที่ด้วยไฟฟ้า):
- การลดน้ำมันเบนซินด้วยไฮโดรเจน (catalytic hydrogenation):
ปฏิกิริยาออกซิเดชัน
เบนซีนเนื่องจากโครงสร้างของมัน มีความทนทานต่อการเกิดออกซิเดชันมาก จึงไม่ได้รับผลกระทบ เช่น โดยสารละลายโพแทสเซียมเปอร์แมงกาเนต อย่างไรก็ตาม การเกิดออกซิเดชันกับแอนไฮไดรด์มาลิกสามารถทำได้โดยใช้ตัวเร่งปฏิกิริยาวาเนเดียมออกไซด์:

- ปฏิกิริยาโอโซน นอกจากนี้ น้ำมันเบนซินยังผ่านกระบวนการโอโซน แต่กระบวนการนี้ช้ากว่าไฮโดรคาร์บอนที่ไม่อิ่มตัว:

ผลของปฏิกิริยาคือการก่อตัวของไดอัลดีไฮด์ - ไกลออกซาล (1,2-ethandial)
- ปฏิกิริยาการเผาไหม้ การเผาไหม้ของเบนซินเป็นกรณีจำกัดของการเกิดออกซิเดชัน น้ำมันเบนซินไวไฟสูงและเผาไหม้ในอากาศด้วยเปลวไฟที่มีควันมาก:
โครงสร้าง
โดยองค์ประกอบ น้ำมันเบนซินเป็นของไฮโดรคาร์บอนไม่อิ่มตัว (อนุกรมคล้ายคลึงกัน น 2น−6) แต่ต่างจากไฮโดรคาร์บอนของซีรีส์เอทิลีน 2 4 มันแสดงคุณสมบัติที่มีอยู่ในไฮโดรคาร์บอนที่ไม่อิ่มตัว (มีลักษณะเฉพาะด้วยปฏิกิริยาการเติม) เฉพาะภายใต้สภาวะที่ไม่เอื้ออำนวย แต่เบนซีนมีแนวโน้มที่จะเกิดปฏิกิริยาทดแทนมากกว่า "พฤติกรรม" ของเบนซีนนี้อธิบายโดยโครงสร้างพิเศษของมัน: การมีอยู่ของอะตอมในระนาบเดียวกันและการมีอยู่ของเมฆอิเล็กตรอน 6π คอนจูเกตในโครงสร้าง แนวคิดสมัยใหม่เกี่ยวกับธรรมชาติของพันธะทางอิเล็กทรอนิกส์ในน้ำมันเบนซินนั้นขึ้นอยู่กับสมมติฐานของ Linus Pauling ผู้เสนอให้วาดภาพโมเลกุลของเบนซีนเป็นรูปหกเหลี่ยมที่มีวงกลมจารึกไว้ซึ่งเน้นว่าไม่มีพันธะคู่คงที่และการมีอยู่ของ เมฆอิเล็กตรอนเดี่ยวครอบคลุมอะตอมของคาร์บอนทั้งหกของวัฏจักร
ในวรรณคดีเฉพาะทางและเป็นที่นิยม คำว่า แหวนเบนซินเกี่ยวข้องกับโครงสร้างคาร์บอนของเบนซินตามกฎโดยไม่คำนึงถึงอะตอมและกลุ่มอื่นที่เกี่ยวข้องกับอะตอมของคาร์บอน วงแหวนเบนซินเป็นส่วนหนึ่งของสารประกอบต่างๆ
การผลิต
ในปัจจุบัน มีวิธีการที่แตกต่างกันหลายประการสำหรับการผลิตน้ำมันเบนซิน

แอปพลิเคชัน

การขนส่งน้ำมันเบนซินโดยทางรถไฟดำเนินการในรถถังเฉพาะทาง
ส่วนสำคัญของน้ำมันเบนซินที่ได้นั้นใช้สำหรับการสังเคราะห์ผลิตภัณฑ์อื่น ๆ :
- น้ำมันเบนซินประมาณ 50% จะถูกแปลงเป็นเอทิลเบนซีน (อัลคิเลชันของเบนซีนกับเอทิลีน);
- น้ำมันเบนซินประมาณ 25% จะถูกแปลงเป็นคิวมีน (อัลคิเลชันของเบนซินกับโพรพิลีน);
- น้ำมันเบนซินประมาณ 10-15% ถูกเติมไฮโดรเจนเป็นไซโคลเฮกเซน
- น้ำมันเบนซินประมาณ 10% ใช้ในการผลิตไนโตรเบนซีน
- น้ำมันเบนซิน 2-3% จะถูกแปลงเป็นอัลคิลเบนซีนเชิงเส้น
- น้ำมันเบนซินประมาณ 1% ใช้สำหรับสังเคราะห์คลอโรเบนซีน
น้ำมันเบนซินถูกใช้เพื่อสังเคราะห์สารประกอบอื่นๆ ในปริมาณที่น้อยกว่ามาก ในบางครั้งและในกรณีที่รุนแรง เนื่องจากมีความเป็นพิษสูง จึงใช้น้ำมันเบนซินเป็นตัวทำละลาย
นอกจากนี้ เบนซินยังเป็นส่วนหนึ่งของน้ำมันเบนซิน ในช่วงทศวรรษที่ 1920 และ 1930 น้ำมันเบนซินถูกเติมเข้าไปในน้ำมันเบนซินแบบวิ่งตรงเพื่อเพิ่มค่าออกเทน แต่ในช่วงทศวรรษที่ 1940 น้ำมันผสมดังกล่าวไม่สามารถแข่งขันกับน้ำมันเบนซินออกเทนสูงได้ เนื่องจากมีความเป็นพิษสูง ปริมาณน้ำมันเบนซินในเชื้อเพลิงจึงถูกจำกัดโดยมาตรฐานสมัยใหม่จนถึง 1%
การกระทำทางชีวภาพและพิษวิทยา
เบนซีนเป็นซีโนไบโอติกของมนุษย์ที่พบได้บ่อยที่สุดชนิดหนึ่ง
เบนซีนเป็นพิษสูง ปริมาณขั้นต่ำที่ร้ายแรงสำหรับการบริหารช่องปากคือ 15 มล. ค่าเฉลี่ยคือ 50-70 มล. ด้วยการสูดดมไอเบนซีนสั้น ๆ จะไม่เกิดพิษในทันทีดังนั้นจนกระทั่งเมื่อเร็ว ๆ นี้ขั้นตอนการทำงานกับน้ำมันเบนซินจึงไม่ได้รับการควบคุมโดยเฉพาะ ในปริมาณมาก น้ำมันเบนซินทำให้เกิดอาการคลื่นไส้และเวียนศีรษะ และในบางกรณีที่รุนแรง พิษอาจถึงแก่ชีวิตได้ สัญญาณแรกของพิษจากน้ำมันเบนซินมักเป็นความอิ่มอกอิ่มใจ ไอเบนซีนสามารถทะลุผ่านผิวหนังที่ไม่บุบสลายได้ น้ำมันเบนซินค่อนข้างระคายเคืองต่อผิวหนัง หากร่างกายมนุษย์สัมผัสกับน้ำมันเบนซินในปริมาณเล็กน้อยในระยะยาว ผลที่ตามมาก็อาจร้ายแรงเช่นกัน
เบนซีนเป็นสารก่อมะเร็งที่รุนแรง การศึกษาแสดงให้เห็นความสัมพันธ์ระหว่างน้ำมันเบนซินกับโรคต่างๆ เช่น โรคโลหิตจางชนิดอะพลาสติก มะเร็งเม็ดเลือดขาวเฉียบพลัน (มัยอีลอยด์ ลิมโฟบลาสติก) มะเร็งเม็ดเลือดขาวเรื้อรังแบบมัยอีลอยด์ โรคไขกระดูก และโรคไขกระดูก
กลไกการแปรสภาพและผลการกลายพันธุ์ของเบนซีน
กลไกการเปลี่ยนแปลงของน้ำมันเบนซินในร่างกายมนุษย์มีหลายรูปแบบ ในตัวแปรแรก โมเลกุลของเบนซีนจะถูกไฮดรอกซีเลตโดยระบบไมโครโซมอลออกซิเดชันโดยมีส่วนร่วมของไซโตโครม P450 ตามกลไกนี้ น้ำมันเบนซินจะถูกออกซิไดซ์เป็นอีพอกไซด์ที่มีปฏิกิริยาสูงก่อน ซึ่งจะถูกแปลงเป็นฟีนอลต่อไป นอกจากนี้ อนุมูลอิสระ (ชนิดของออกซิเจนที่ทำปฏิกิริยา) ถูกสร้างขึ้นเนื่องจากการกระตุ้น P450 สูงตามปฏิกิริยา:
กลไกระดับโมเลกุลของการกลายพันธุ์ของเบนซีน
เบนซินคือ promutagenมันได้มาซึ่งคุณสมบัติในการกลายพันธุ์หลังจากการเปลี่ยนรูปทางชีวภาพเท่านั้นซึ่งเป็นผลมาจากสารประกอบที่มีปฏิกิริยาสูงเกิดขึ้น หนึ่งในนั้นคือเบนซีนอีพอกไซด์ เนื่องจากความเค้นเชิงมุมสูงของวัฏจักรอีพอกซี พันธะ -C-O-C- จะแตกตัวและโมเลกุลจะกลายเป็นอิเล็กโทรไฟล์ มันทำปฏิกิริยากับศูนย์กลางนิวคลีโอฟิลิกของเบสไนโตรเจนของโมเลกุลกรดนิวคลีอิกได้อย่างง่ายดาย โดยเฉพาะอย่างยิ่ง DNA
กลไกการทำงานร่วมกันของวัฏจักรอีพอกซีกับศูนย์นิวคลีโอฟิลิก - กลุ่มอะมิโนของเบสไนโตรเจน (ปฏิกิริยาอะริเลชัน) ดำเนินการเป็นปฏิกิริยาการแทนที่นิวคลีโอฟิลิก 2 . เป็นผลให้เกิด DNA adducts ที่จับกับโควาเลนต์ที่ค่อนข้างแรง อนุพันธ์ดังกล่าวมักพบใน guanine (เนื่องจากโมเลกุลของ guanine มี จำนวนเงินสูงสุดศูนย์นิวคลีโอฟิลิก) ตัวอย่างเช่น N7-ฟีนิลกัวนีน DNA adducts ที่เป็นผลลัพธ์สามารถนำไปสู่การเปลี่ยนแปลงในโครงสร้างดั้งเดิมของ DNA ซึ่งจะรบกวนการถอดรหัสและการจำลองแบบที่เหมาะสม อะไรคือที่มาของการกลายพันธุ์ทางพันธุกรรม. การสะสมของอีพอกไซด์ในเซลล์ตับ (เซลล์ตับ) นำไปสู่ผลที่ไม่อาจย้อนกลับได้: การเพิ่มขึ้นของ DNA arylation และในขณะเดียวกันการแสดงออก (overexpression) ของโปรตีนกลายพันธุ์ที่เพิ่มขึ้นซึ่งเป็นผลิตภัณฑ์ของการกลายพันธุ์ทางพันธุกรรม การยับยั้งการตายของเซลล์ การเปลี่ยนแปลงของเซลล์และแม้กระทั่งความตาย นอกจากความเป็นพิษต่อยีนและการกลายพันธุ์ที่เด่นชัดแล้ว เบนซินยังมีพิษต่อกล้ามเนื้อและฤทธิ์ก่อมะเร็งที่รุนแรง โดยเฉพาะอย่างยิ่งผลกระทบนี้ปรากฏในเซลล์ของเนื้อเยื่อไมอีลอยด์ (เซลล์ของเนื้อเยื่อนี้ไวต่อผลกระทบของซีโนไบโอติกมาก)
สารเบนซีนและสารเสพติด
น้ำมันเบนซินมีผลที่น่าตกใจกับบุคคลและอาจนำไปสู่การติดยาได้
พิษเฉียบพลัน
ที่ความเข้มข้นสูงมาก - เกือบจะหมดสติและเสียชีวิตทันทีภายในไม่กี่นาที ใบหน้าเป็นสีฟ้า เยื่อเมือกมักเป็นสีแดงเชอร์รี่ ที่ความเข้มข้นต่ำกว่า - กระตุ้น, คล้ายกับแอลกอฮอล์, แล้วง่วงซึม, อ่อนแอทั่วไป, เวียนศีรษะ, คลื่นไส้, อาเจียน, ปวดหัว, หมดสติ นอกจากนี้ยังสังเกตเห็นการกระตุกของกล้ามเนื้อซึ่งสามารถเปลี่ยนเป็นอาการชักได้ รูม่านตามักจะขยายและไม่ตอบสนองต่อแสง การหายใจจะเร็วขึ้นก่อนแล้วจึงช้าลง อุณหภูมิร่างกายลดลงอย่างรวดเร็ว ชีพจรเต้นเร็วขึ้น เติมขนาดเล็ก ความดันโลหิตจะลดลง มีรายงานกรณีของภาวะหัวใจเต้นผิดจังหวะรุนแรง
หลังจากพิษรุนแรงที่ไม่นำไปสู่ความตายโดยตรงบางครั้งอาจสังเกตเห็นความผิดปกติด้านสุขภาพ: เยื่อหุ้มปอดอักเสบ, โรคหวัดของระบบทางเดินหายใจส่วนบน, โรคของกระจกตาและเรตินา, ความเสียหายของตับ, ความผิดปกติของหัวใจ ฯลฯ กรณีของ vasomotor โรคประสาทที่มีอาการบวมที่ใบหน้าและแขนขา ความไวต่อความผิดปกติและการชักหลังจากพิษจากไอเบนซีนเฉียบพลัน บางครั้งความตายเกิดขึ้นภายหลังการได้รับพิษ
พิษเรื้อรัง
ในกรณีที่รุนแรง ได้แก่ ปวดศีรษะ เหนื่อยล้าอย่างรุนแรง หายใจลำบาก เวียนศีรษะ อ่อนแอ หงุดหงิด ง่วงนอนหรือนอนไม่หลับ อาหารไม่ย่อย คลื่นไส้ อาเจียนเป็นบางครั้ง เบื่ออาหาร ปัสสาวะเพิ่มขึ้น มีประจำเดือน มีเลือดออกถาวรจากเยื่อเมือกในช่องปาก โดยเฉพาะ เหงือกมักจะพัฒนา , และจมูก ยาวนานเป็นชั่วโมงหรือเป็นวัน บางครั้งเลือดออกต่อเนื่องเกิดขึ้นหลังจากการถอนฟัน เลือดออกเล็กน้อยจำนวนมาก (ตกเลือด) ในผิวหนัง เลือดในอุจจาระ เลือดออกในโพรงมดลูก เลือดออกในจอประสาทตา โดยปกติจะมีเลือดออกและมักมีไข้ (อุณหภูมิสูงถึง 40 °ขึ้นไป) ที่นำพิษมาที่โรงพยาบาล ในกรณีเช่นนี้ การพยากรณ์โรคมักเป็นเรื่องร้ายแรง สาเหตุของการตายบางครั้งคือการติดเชื้อทุติยภูมิ: มีหลายกรณีของการอักเสบที่เป็นเนื้อตายของเชิงกรานและเนื้อร้ายของกราม, การอักเสบที่รุนแรงของเหงือก, ภาวะติดเชื้อในโพรงมดลูกทั่วไปที่มีภาวะเยื่อบุโพรงมดลูกอักเสบ
บางครั้งเมื่อได้รับพิษรุนแรงอาการของโรคประสาทจะเกิดขึ้น: การตอบสนองของเอ็นเพิ่มขึ้น, โคลนัสทวิภาคี, อาการ Babinsky เชิงบวก, ความผิดปกติของความไวลึก, ความผิดปกติของแท็บหลอกด้วยความรู้สึกผิดปกติ, ataxia, อัมพาตครึ่งซีกและความผิดปกติของมอเตอร์ (สัญญาณของความเสียหายต่อ คอลัมน์หลังของไขสันหลังและทางเดินเสี้ยม)
การเปลี่ยนแปลงในเลือดโดยทั่วไป โดยปกติจำนวนเม็ดเลือดแดงจะลดลงอย่างรวดเร็วเหลือ 1-2 ล้านหรือต่ำกว่า เนื้อหาของเฮโมโกลบินยังลดลงอย่างรวดเร็วบางครั้งถึง 10% ดัชนีสีในบางกรณีอาจต่ำ บางครั้งใกล้เคียงกับปกติ และบางครั้งสูง (โดยเฉพาะอย่างยิ่งกับภาวะโลหิตจางรุนแรง) มีการระบุ Anisocytosis และ poikilocytosis, การเจาะ basophilic และการปรากฏตัวของเม็ดเลือดแดงนิวเคลียร์, การเพิ่มจำนวนของ reticulocytes และปริมาตรของเม็ดเลือดแดง จำนวนเม็ดเลือดขาวลดลงอย่างรวดเร็วเป็นเรื่องปกติมากขึ้น บางครั้งในตอนแรก leukocytosis, leukopenia ถูกแทนที่อย่างรวดเร็ว, เร่ง ESR การเปลี่ยนแปลงในเลือดไม่ได้เกิดขึ้นพร้อมกัน ส่วนใหญ่มักระบบเม็ดโลหิตขาวได้รับผลกระทบก่อนหน้านี้ thrombocytopenia เข้าร่วมในภายหลัง ความพ่ายแพ้ของการทำงานของเม็ดเลือดแดงมักเกิดขึ้นภายหลัง ในอนาคตอาจเกิดภาพลักษณะเฉพาะของพิษร้ายแรง - โรคโลหิตจาง aplastic
ผลของพิษอาจยังคงอยู่และแม้กระทั่งเดือนและปีหลังจากหยุดทำงานกับเบนซิน
การปฐมพยาบาลสำหรับการเป็นพิษและการรักษา
ในกรณีที่เป็นพิษเฉียบพลันจากน้ำมันเบนซิน (ไอเบนซีน) เหยื่อจะต้องถูกนำออกไปในที่ที่มีอากาศบริสุทธิ์ก่อนในกรณีที่ระบบทางเดินหายใจหยุดหายใจการช่วยหายใจจะดำเนินการเพื่อทำให้ปกติใช้ออกซิเจนและ lobeline เป็นตัวกระตุ้นระบบทางเดินหายใจ ห้ามใช้อะดรีนาลีนเป็นยาแก้ปวดโดยเด็ดขาด! หากอาเจียน ให้ฉีดสารละลายน้ำตาลกลูโคส 40% ทางหลอดเลือดดำ ในกรณีที่ระบบไหลเวียนเลือดผิดปกติ - การฉีดสารละลายคาเฟอีน หากพิษเกิดขึ้นทางปากและเบนซินเข้าไปในกระเพาะอาหารจำเป็นต้องล้างด้วยน้ำมันพืช (เบนซินดูดซับได้ดี) ขั้นตอนนี้ควรดำเนินการด้วยความระมัดระวังเนื่องจากอาจเกิดการสำลักได้ ด้วยพิษเล็กน้อยผู้ป่วยจะได้รับการพักผ่อน ในสภาวะตื่นเต้นจำเป็นต้องใช้ยาระงับประสาท ในกรณีของโรคโลหิตจาง, การถ่ายเลือด, วิตามินบี 12, กรดโฟลิกจะดำเนินการ, ในกรณีของเม็ดเลือดขาว - วิตามินบี 6, เพนทอกซิล ในกรณีที่ภูมิคุ้มกันลดลง (สถานะภูมิคุ้มกันบกพร่อง) - สารกระตุ้นภูมิคุ้มกัน
การกระทำของเบนซีนต่อไบโอเมมเบรน
เยื่อหุ้มชีวภาพเป็นโครงสร้างซุปเปอร์โมเลกุล - ชั้นไขมันสองเท่าซึ่งถูกรวม (ฝัง) หรือติดอยู่บนพื้นผิวของโมเลกุลของโปรตีนโพลีแซคคาไรด์ ลิพิดที่ประกอบเป็นไบโอแมมเบรนนั้นโดยธรรมชาติแล้วเป็นสารประกอบแอมฟิฟิลิค (อะโมฟีลิก) นั่นคือสามารถละลายได้ทั้งในสารที่มีขั้วและไม่ใช่ขั้ว เนื่องจากการมีอยู่ของกลุ่มขั้วในพวกมัน ที่เรียกว่า "ศีรษะ"(คาร์บอกซิลิก -COOH, ไฮดรอกซิล -OH, หมู่อะมิโน -NH 2 และอื่นๆ) และสิ่งที่เรียกว่าไม่มีขั้ว "หาง"(อนุมูลไฮโดรคาร์บอน - อัลคิล, แอริล, โครงสร้างโพลีไซคลิกเช่น cholestan และอื่น ๆ )
เบนซีนเป็นสารช่วยละลายเยื่อหุ้มชีวภาพอย่างมีประสิทธิภาพ โดยจะละลายกลุ่มที่ไม่มีขั้ว (ที่เรียกว่าไฮโดรคาร์บอน) อย่างรวดเร็ว "หาง") ไขมันซึ่งส่วนใหญ่เป็นคอเลสเตอรอลซึ่งเป็นส่วนหนึ่งของเยื่อหุ้มเซลล์ กระบวนการละลายถูกจำกัดโดยความเข้มข้นของเบนซีน ยิ่งกระบวนการนี้ดำเนินไปเร็วขึ้นเท่านั้น ในกระบวนการของการละลาย พลังงานจะถูกปลดปล่อยออกมา ทำลายชั้นไขมันสองชั้น (ลิปิด ไบเลเยอร์) อย่างแท้จริง ซึ่งนำไปสู่การทำลายอย่างสมบูรณ์ (การทำลายโครงสร้าง) ของเมมเบรนและการตายของเซลล์ที่ตามมา (ในระหว่างการทำลายของไบโอแมมเบรน ตัวรับเมมเบรนจะถูกกระตุ้น (เช่น เช่น CD95, TNFR1, DR3, DR4 และอื่นๆ) ที่กระตุ้นการตายของเซลล์)
ออกฤทธิ์ต่อผิวหนัง
เมื่อสัมผัสกับน้ำมันเบนซินบ่อยครั้ง ผิวแห้ง รอยแตก อาการคัน รอยแดง (โดยปกติระหว่างนิ้วมือ) อาการบวมและตุ่มคล้ายลูกเดือย บางครั้งเนื่องจากแผลที่ผิวหนัง พนักงานถูกบังคับให้ออกจากงาน
ความเข้มข้นสูงสุดที่อนุญาตคือ 5 มก./ม. 3
ความปลอดภัย
การทำงานกับน้ำมันเบนซินมีความเสี่ยงที่จะเกิดพิษและปัญหาสุขภาพที่ร้ายแรง เบนซีนเป็นของเหลวที่มีความผันผวนสูง (ความผันผวน 320 มก. / ล. ที่ 20 ° C) ที่มีความไวไฟสูง ดังนั้นเมื่อทำงานกับมัน จำเป็นต้องปฏิบัติตามข้อควรระวังเพื่อความปลอดภัยในการทำงานกับของเหลวที่ติดไฟได้ ไอระเหยของน้ำมันเบนซินเป็นอันตรายอย่างยิ่ง เนื่องจากสามารถก่อให้เกิดส่วนผสมที่ระเบิดได้กับอากาศ ในปัจจุบัน การใช้น้ำมันเบนซินเป็นตัวทำละลายอินทรีย์มีจำกัดอย่างมาก เนื่องจากความเป็นพิษและผลการก่อมะเร็งของไอระเหยและผลกระทบด้านลบต่อผิวหนัง การทำงานกับน้ำมันเบนซินในห้องปฏิบัติการยังมีข้อจำกัดอีกด้วย (ควบคุมอย่างเข้มงวด) แนะนำให้ใช้น้ำมันเบนซินในการทดลองในปริมาณน้อยเท่านั้น (ไม่เกิน 50 มล.) ควรใช้ถุงมือฟลูออรีนเท่านั้น (น้ำยางจะละลายและบวมเมื่อสัมผัสกับน้ำมันเบนซิน)
- เก็บใกล้แหล่งความร้อน เปลวไฟ ตัวออกซิไดซ์อย่างแรง ผลิตภัณฑ์อาหารฯลฯ
- ทิ้งภาชนะที่บรรจุน้ำมันเบนซินไว้ เปิดควัน
- ใช้ถังน้ำมันเบนซินสำหรับอาหาร ล้างมือ จาน
- ทำงานในห้องที่ปิดและมีอากาศถ่ายเทไม่ดีโดยมีอุณหภูมิอากาศมากกว่า 30 ° C
- ใช้สารปริมาณมากเป็นตัวทำละลาย
- ทำงานโดยไม่มีอุปกรณ์ป้องกันผิวหนังของมือ ตา และอวัยวะระบบทางเดินหายใจ
นิเวศวิทยา
เบนซีนเป็นสารที่ไม่ปลอดภัยต่อสิ่งแวดล้อม เป็นพิษจากแหล่งกำเนิดของมนุษย์ แหล่งที่มาหลักของน้ำมันเบนซินเข้าสู่ สิ่งแวดล้อมที่มีการปล่อยน้ำเสียหรืออากาศ ได้แก่ อุตสาหกรรมปิโตรเคมีและโค้ก การผลิตเชื้อเพลิงและการขนส่ง จากแหล่งกักเก็บ น้ำมันเบนซินระเหยง่าย สามารถเปลี่ยนจากดินเป็นพืชได้ ซึ่งเป็นภัยคุกคามร้ายแรงต่อระบบนิเวศ
น้ำมันเบนซินมีคุณสมบัติในการสะสมเนื่องจากความเป็นไขมันจึงสามารถสะสมในเซลล์ของเนื้อเยื่อไขมันของสัตว์ได้จึงเป็นพิษ
ปฏิกิริยากลุ่มแรกคือปฏิกิริยาการแทนที่ เรากล่าวว่า arenes ไม่มีพันธะหลายอันในโครงสร้างโมเลกุล แต่มีระบบคอนจูเกตที่มีอิเล็กตรอน 6 ตัว ซึ่งมีความเสถียรมากและให้ความแข็งแรงเพิ่มเติมแก่วงแหวนเบนซีน ดังนั้นใน ปฏิกริยาเคมีการเปลี่ยนอะตอมไฮโดรเจนจะเกิดขึ้นก่อน ไม่ใช่การทำลายวงแหวนเบนซิน
เราได้พบปฏิกิริยาการแทนที่เมื่อพูดถึงอัลเคนแล้ว แต่สำหรับพวกมัน ปฏิกิริยาเหล่านี้ดำเนินไปตามกลไกที่ต่างไปจากเดิมอย่างสิ้นเชิง ในขณะที่ arenes มีลักษณะเฉพาะด้วยกลไกไอออนิกของปฏิกิริยาการแทนที่
อันดับแรกคุณสมบัติทางเคมี - ฮาโลเจน การแทนที่ของอะตอมไฮโดรเจนสำหรับอะตอมของฮาโลเจน - คลอรีนหรือโบรมีน
ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อนและมีส่วนร่วมของตัวเร่งปฏิกิริยาเสมอ ในกรณีของคลอรีนก็อาจเป็นอะลูมิเนียมคลอไรด์หรือเหล็กคลอไรด์สามชนิด ตัวเร่งปฏิกิริยาโพลาไรซ์โมเลกุลของฮาโลเจน ส่งผลให้เกิดการแตกพันธะเฮเทอโรไลติกและได้ไอออน
คลอไรด์ไอออนที่มีประจุบวกทำปฏิกิริยากับเบนซิน
หากเกิดปฏิกิริยากับโบรมีน เหล็กไตรโบรไมด์หรืออะลูมิเนียมโบรไมด์จะทำหน้าที่เป็นตัวเร่งปฏิกิริยา

สิ่งสำคัญคือต้องสังเกตว่าปฏิกิริยาเกิดขึ้นกับโมเลกุลโบรมีน ไม่ใช่กับน้ำโบรมีน เบนซีนไม่ทำปฏิกิริยากับน้ำโบรมีน
การเกิดฮาโลเจนของสารคล้ายคลึงกันเบนซินมีลักษณะเฉพาะของตัวเอง ในโมเลกุลโทลูอีน กลุ่มเมทิลอำนวยความสะดวกในการแทนที่ในวงแหวน การเกิดปฏิกิริยาเพิ่มขึ้น และปฏิกิริยาดำเนินไปภายใต้สภาวะที่รุนแรงกว่า นั่นคือที่อุณหภูมิห้องอยู่แล้ว

สิ่งสำคัญคือต้องสังเกตว่าการแทนที่จะเกิดขึ้นในตำแหน่งออร์โธและพาราเสมอ ดังนั้นจึงได้ส่วนผสมของไอโซเมอร์
ที่สองคุณสมบัติ - ไนเตรตของเบนซินการแนะนำกลุ่มไนโตรลงในวงแหวนเบนซิน

ของเหลวสีเหลืองหนักที่มีกลิ่นอัลมอนด์ขมก่อตัวขึ้น - ไนโตรเบนซีนดังนั้นปฏิกิริยานี้จึงเป็นคุณภาพของน้ำมันเบนซิน สำหรับไนเตรตจะใช้ส่วนผสมไนเตรตของกรดไนตริกและกรดซัลฟิวริกเข้มข้น ปฏิกิริยาจะดำเนินการโดยความร้อน
ฉันขอเตือนคุณว่าสำหรับไนเตรตของอัลเคนในปฏิกิริยา Konovalov กรดไนตริกเจือจางถูกใช้โดยไม่ต้องเติมกรดซัลฟิวริก
ในไนเตรตของโทลูอีน เช่นเดียวกับในฮาโลเจน จะเกิดส่วนผสมของออร์โธ-และพารา-ไอโซเมอร์

ที่สามคุณสมบัติ - อัลคิเลชั่นของเบนซีนกับฮาโลอัลเคน
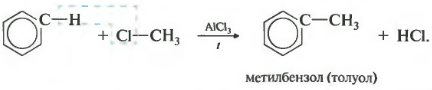
ปฏิกิริยานี้ยอมให้มีการนำไฮโดรคาร์บอนเรดิคัลเข้าไปในวงแหวนเบนซีนและถือได้ว่าเป็นวิธีการเพื่อให้ได้เบนซีนที่คล้ายคลึงกัน อะลูมิเนียมคลอไรด์ถูกใช้เป็นตัวเร่งปฏิกิริยาซึ่งส่งเสริมการสลายตัวของโมเลกุลฮาโลอัลเคนให้เป็นไอออน นอกจากนี้ยังต้องการความร้อน
ที่สี่คุณสมบัติ - alkylation ของเบนซินกับอัลคีน

ด้วยวิธีนี้ ตัวอย่างเช่น สามารถรับคิวมีนหรือเอทิลเบนซีนได้ ตัวเร่งปฏิกิริยาคืออะลูมิเนียมคลอไรด์
2. ปฏิกิริยาการเติมเบนซิน
ปฏิกิริยากลุ่มที่สองคือปฏิกิริยาบวก เรากล่าวว่าปฏิกิริยาเหล่านี้ไม่ใช่ลักษณะเฉพาะ แต่เกิดขึ้นได้ภายใต้สภาวะที่ค่อนข้างรุนแรงด้วยการทำลายเมฆ pi-electron และการเกิดพันธะซิกมา 6 พันธะ
ที่ห้าคุณสมบัติในรายการทั่วไป - ไฮโดรจิเนชัน, การเติมไฮโดรเจน
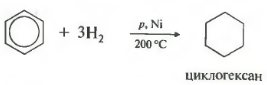
อุณหภูมิ ความดัน ตัวเร่งปฏิกิริยานิกเกิลหรือแพลตตินั่ม โทลูอีนสามารถตอบสนองในลักษณะเดียวกัน
ที่หกคุณสมบัติ - คลอรีน โปรดทราบว่าเรากำลังพูดถึงปฏิกิริยากับคลอรีนโดยเฉพาะ เนื่องจากโบรมีนไม่ทำปฏิกิริยานี้
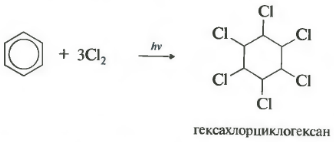
ปฏิกิริยาเกิดขึ้นภายใต้การฉายรังสีอัลตราไวโอเลตอย่างหนัก เฮกซาคลอโรไซโคลเฮกเซน เป็นอีกชื่อหนึ่งของเฮกซาคลอเรน ก่อตัวเป็นของแข็ง
สิ่งสำคัญคือต้องจำไว้ว่าสำหรับเบนซิน เป็นไปไม่ได้ปฏิกิริยาการเติมไฮโดรเจนเฮไลด์ (ไฮโดรฮาโลจิเนชัน) และการเติมน้ำ (ไฮเดรชั่น)
3. การแทนที่ในห่วงโซ่ด้านข้างของ homologues เบนซิน
ปฏิกิริยากลุ่มที่สามเกี่ยวข้องกับความคล้ายคลึงกันของเบนซินเท่านั้น - นี่คือการแทนที่ในห่วงโซ่ด้านข้าง
ที่เจ็ดคุณสมบัติในรายการทั่วไปคือฮาโลเจนที่อะตอมอัลฟาคาร์บอนในสายด้านข้าง

ปฏิกิริยาจะเกิดขึ้นเมื่อถูกความร้อนหรือถูกฉายรังสี และมักจะเกิดขึ้นที่อัลฟาคาร์บอนเท่านั้น ในขณะที่ฮาโลเจนดำเนินต่อไป อะตอมของฮาโลเจนที่สองจะกลับสู่ตำแหน่งอัลฟา
4. การเกิดออกซิเดชันของสารคล้ายคลึงกันเบนซิน
ปฏิกิริยากลุ่มที่สี่คือการเกิดออกซิเดชัน
แหวนเบนซินแรงเกินไปดังนั้นเบนซิน ไม่ออกซิไดซ์โพแทสเซียมเปอร์แมงกาเนต - ไม่เปลี่ยนสีของสารละลาย นี่เป็นสิ่งสำคัญมากที่ต้องจำ
ในทางกลับกัน homologues ของเบนซีนจะถูกออกซิไดซ์ด้วยสารละลายโพแทสเซียมเปอร์แมงกาเนตที่เป็นกรดเมื่อถูกความร้อน และนี่คือคุณสมบัติทางเคมีที่แปด

ปรากฎว่ากรดเบนโซอิก มีการสังเกตการเปลี่ยนสีของสารละลาย ในกรณีนี้ ไม่ว่าสายโซ่คาร์บอนของหมู่แทนที่จะยาวแค่ไหน มันก็แตกสลายหลังจากอะตอมของคาร์บอนแรกเสมอ และอะตอมอัลฟ่าจะถูกออกซิไดซ์เป็นหมู่คาร์บอกซิลด้วยการก่อตัวของกรดเบนโซอิก โมเลกุลที่เหลือจะถูกออกซิไดซ์เป็นกรดที่สอดคล้องกันหรือถ้าเป็นอะตอมของคาร์บอนเพียงอะตอมเดียว to คาร์บอนไดออกไซด์.
หากคล้ายคลึงกันของเบนซีนมีสารแทนที่ไฮโดรคาร์บอนมากกว่าหนึ่งตัวบนวงแหวนอะโรมาติก การเกิดออกซิเดชันจะเกิดขึ้นตามกฎเดียวกัน - คาร์บอนในตำแหน่งอัลฟ่าจะถูกออกซิไดซ์

ในตัวอย่างนี้ จะได้กรดอะโรมาติกไดบาซิก ซึ่งเรียกว่ากรดพาทาลิก
ด้วยวิธีพิเศษ ฉันสังเกตการเกิดออกซิเดชันของคิวมีน ไอโซโพรพิลเบนซีนด้วยออกซิเจนในบรรยากาศต่อหน้ากรดซัลฟิวริก

นี่เป็นวิธีที่เรียกว่าคิวมีนในการผลิตฟีนอล ตามกฎแล้วเราต้องจัดการกับปฏิกิริยานี้ในเรื่องที่เกี่ยวข้องกับการผลิตฟีนอล นี่คือวิถีทางอุตสาหกรรม
เก้าคุณสมบัติ - การเผาไหม้, ออกซิเดชันสมบูรณ์ด้วยออกซิเจน น้ำมันเบนซินและสารคล้ายคลึงกันเผาไหม้เป็นคาร์บอนไดออกไซด์และน้ำ
ให้เราเขียนสมการการเผาไหม้เบนซินในรูปแบบทั่วไป
ตามกฎการอนุรักษ์มวล ควรมีอะตอมทางด้านซ้ายมากที่สุดเท่าที่มีอะตอมทางด้านขวา เพราะในปฏิกิริยาเคมี อะตอมไม่ได้ไปไหน แต่ลำดับของพันธะระหว่างพวกมันก็เปลี่ยนไป ดังนั้นจะมีโมเลกุลของคาร์บอนไดออกไซด์มากพอๆ กับที่มีอะตอมของคาร์บอนในโมเลกุลของอารีน เนื่องจากโมเลกุลนั้นมีอะตอมของคาร์บอนอยู่หนึ่งอะตอม นั่นคือโมเลกุล n CO 2 จะมีโมเลกุลของน้ำครึ่งหนึ่งเท่ากับอะตอมไฮโดรเจน นั่นคือ (2n-6) / 2 ซึ่งหมายถึง n-3
มีจำนวนอะตอมออกซิเจนเท่ากันทางด้านซ้ายและด้านขวา ทางด้านขวามีคาร์บอนไดออกไซด์อยู่ 2n เนื่องจากแต่ละโมเลกุลมีออกซิเจน 2 อะตอม บวกกับ n-3 จากน้ำ รวมเป็น 3n-3 ทางด้านซ้ายมีอะตอมออกซิเจนจำนวนเท่ากัน - 3n-3 ซึ่งหมายความว่ามีโมเลกุลจำนวนครึ่งหนึ่งเนื่องจากโมเลกุลประกอบด้วยอะตอมสองอะตอม นั่นคือ (3n-3)/2 โมเลกุลออกซิเจน
ดังนั้นเราจึงได้รวบรวมสมการการเผาไหม้ของสารคล้ายคลึงเบนซีนในรูปแบบทั่วไป
Arenes เป็นอะโรมาติกไฮโดรคาร์บอนที่มีวงแหวนเบนซินหนึ่งวงขึ้นไป วงแหวนเบนซินประกอบด้วยอะตอมของคาร์บอน 6 อะตอม ซึ่งพันธะคู่และพันธะเดี่ยวจะสลับกัน
สิ่งสำคัญคือต้องสังเกตว่าพันธะคู่ในโมเลกุลเบนซีนไม่คงที่ แต่จะเคลื่อนที่เป็นวงกลมอย่างต่อเนื่อง
Arenes เรียกอีกอย่างว่าอะโรมาติกไฮโดรคาร์บอน สมาชิกคนแรก ซีรีส์ที่คล้ายคลึงกัน- เบนซิน - C 6 H 6 . สูตรทั่วไปสำหรับอนุกรมคล้ายคลึงกันคือ C n H 2n-6
เป็นเวลานานที่สูตรโครงสร้างของเบนซินยังคงเป็นปริศนา สูตรที่ Kekule เสนอด้วยพันธะสามสองพันธะไม่สามารถอธิบายความจริงที่ว่าน้ำมันเบนซินไม่ทำปฏิกิริยาเพิ่มเติม ดังที่ได้กล่าวไว้ข้างต้น ตามแนวคิดสมัยใหม่ พันธะคู่ในโมเลกุลจะเคลื่อนที่อยู่ตลอดเวลา ดังนั้นจึงเป็นการถูกต้องกว่าที่จะวาดพวกมันในรูปของวงแหวน
พันธะคู่ก่อให้เกิดการผันคำกริยาในโมเลกุลเบนซีน อะตอมของคาร์บอนทั้งหมดอยู่ในสถานะของการผสมแบบ sp 2 มุมวาเลนซ์ - 120 °
ศัพท์เฉพาะและ isomerism ของ arenes
ชื่อของ arenes เกิดขึ้นจากการเพิ่มชื่อของหมู่แทนที่ในสายโซ่หลัก - วงแหวนเบนซีน: เบนซิน, เมทิลเบนซีน (โทลูอีน), เอทิลเบนซีน, โพรพิลเบนซีน ฯลฯ ตามปกติแล้ว สารทดแทนจะเรียงตามลำดับตัวอักษร หากมีส่วนประกอบหลายอย่างในวงแหวนเบนซิน ให้เลือกเส้นทางที่สั้นที่สุดระหว่างวงแหวนดังกล่าว

Arenes มีลักษณะเฉพาะโดย isomerism เชิงโครงสร้างที่เกี่ยวข้องกับตำแหน่งของหมู่แทนที่ ตัวอย่างเช่น สองหมู่แทนที่บนวงแหวนเบนซินอาจอยู่ในตำแหน่งที่ต่างกัน
ชื่อของตำแหน่งของสารทดแทนในวงแหวนเบนซินนั้นเกิดขึ้นจากตำแหน่งของพวกมันที่สัมพันธ์กัน มันแสดงโดยคำนำหน้า ortho-, meta- และ para ด้านล่างนี้คุณจะพบคำแนะนำช่วยในการจำสำหรับการท่องจำที่ประสบความสำเร็จ;)

รับอารีน่า
สามารถรับ Arenas ได้หลายวิธี:

คุณสมบัติทางเคมีของ arenes
Arenes เป็นอะโรมาติกไฮโดรคาร์บอนที่มีวงแหวนเบนซินที่มีพันธะคู่แบบคอนจูเกต คุณลักษณะนี้ทำให้ปฏิกิริยาการเติมทำได้ยาก (แต่ยังคงเป็นไปได้!)
โปรดจำไว้ว่า เบนซีนและสารที่คล้ายคลึงกันไม่เหมือนกับสารประกอบไม่อิ่มตัวอื่นๆ จะไม่เปลี่ยนสีน้ำโบรมีนและสารละลายโพแทสเซียมเปอร์แมงกาเนต

© Bellevich Yury Sergeevich 2018-2020
บทความนี้เขียนโดย Yury Sergeevich Bellevich และเป็นทรัพย์สินทางปัญญาของเขา การคัดลอก แจกจ่าย (รวมถึงการคัดลอกไปยังไซต์และแหล่งข้อมูลอื่นบนอินเทอร์เน็ต) หรือการใช้ข้อมูลและวัตถุอื่นใดโดยไม่ได้รับความยินยอมล่วงหน้าจากผู้ถือลิขสิทธิ์มีโทษตามกฎหมาย ในการขอรับเนื้อหาของบทความและการอนุญาตให้ใช้ โปรดติดต่อ